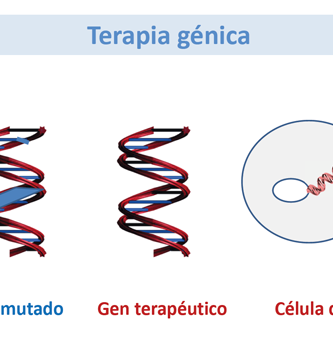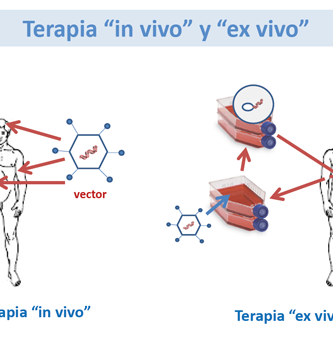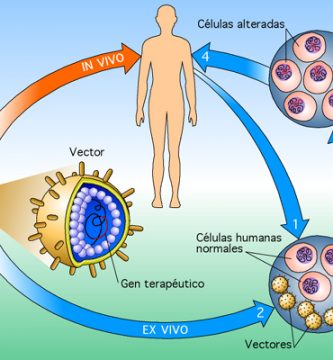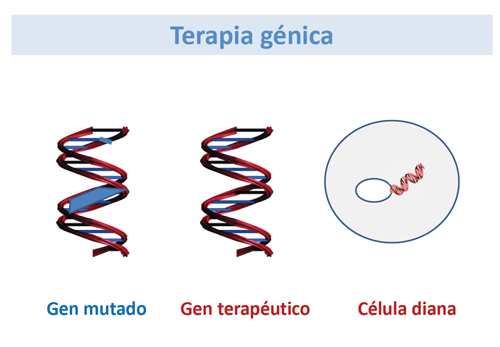
Existen muchas condiciones que deben cumplirse para permitir que la terapia génica sea posible. Primero, los detalles del proceso de la enfermedad deben ser entendidos. Por supuesto, los científicos deben saber exactamente qué gen es defectuoso, pero también cuándo y a qué nivel ese gen se expresaría normalmente, cómo funciona y cuáles son las posibilidades regenerativas para el tejido afectado. No todas las enfermedades pueden ser tratadas con terapia génica. Debe quedar claro que la sustitución del gen defectuoso beneficiaría al paciente. Por ejemplo, una mutación que conduce a un defecto de nacimiento podría ser imposible de tratar, ya que el daño irreversible ya ha ocurrido en el momento en que el paciente es identificado. Del mismo modo, las enfermedades que causan la muerte de las células cerebrales no son adecuadas para la terapia génica: Aunque la terapia génica podría ser capaz de detener la progresión de la enfermedad, el daño existente no se puede revertir porque las células cerebrales no pueden regenerarse. Además, las células a las que se debe entregar al ADN deben ser accesibles. Finalmente, se justifica una gran precaución a medida que se persigue la terapia génica, ya que la respuesta del organismo a altas dosis de vectores virales puede ser impredecible. El 12 de septiembre de 1999, Jesse Gelsinger, un participante de dieciocho años en un ensayo clínico en Filadelfia, se enfermó inesperadamente y murió de los efectos secundarios de la administración hepática de adenovirus. Esta tragedia ilustra la importancia de una atención cuidadosa a las regulaciones de seguridad y extensos experimentos en sistemas de modelos animales antes de pasar a ensayos clínicos humanos.
Distrofias Musculares
Duchenne y otras distrofias musculares recesivas son bien adecuadas en muchos sentidos para la terapia génica. Estas son enfermedades genéticas recesivas de pérdida de función causadas por mutaciones en el gen de la distrofina o en genes para otras proteínas musculares estructurales. Los niveles normales de estas proteínas son conocidos, al igual que muchas de las formas en que funcionan en la célula muscular. Existe una amplia evidencia en sistemas de modelos animales de que estas enfermedades pueden curarse mediante la entrega de copias funcionales del gen. Esto es cierto en gran parte porque el tejido muscular tiene una tremenda capacidad de reparación y regeneración, por lo que se podría imaginar que el músculo fuertemente dañado podría repararse después de la transferencia de genes con éxito. El tejido muscular es también un excelente objetivo para la transferencia de genes.
Se han utilizado varios enfoques diferentes para transferir ADN al músculo. El enfoque más directo es la inyección intramuscular directa de ADN en forma circular denominada plásmido. La ventaja de este enfoque es que induce poca o ninguna respuesta inmune, aunque el número total de células que expresan el gen es bastante bajo. Por el contrario, los adenovirus recombinantes son extremadamente eficientes en la transferencia de genes al músculo, pero dan lugar a una potente respuesta inmune que da como resultado sólo una expresión a corto plazo de los genes transferidos. Debido a que la eficacia de la transferencia de adenovirus es tan grande, se están realizando enormes esfuerzos para reducir la inmunogenicidad de estos vectores. Estos esfuerzos han producido algunos vectores significativamente mejorados, y la investigación se centra ahora en el desarrollo de métodos para preparar las grandes cantidades necesarias para el uso clínico. El virus adeno-asociado combina la eficacia extremadamente alta de la transferencia adenoviral con la muy baja inmunogenicidad de la transferencia directa de ADN. Sin embargo, este virus tiene una capacidad bastante pequeña para transportar ADN, tan pequeño que no puede portar el gen de la distrofina (uno de los genes más grandes conocidos), que se necesita para tratar la distrofia muscular de Duchenne.
Enfermedad de hemofilia y de células falciformes
Debido a la dificultad en el tratamiento de enfermedades como la distrofia muscular, muchos investigadores han optado por centrarse en enfermedades genéticas que pueden ser más fáciles de tratar, en particular las que resultan de la falta de proteínas libremente disueltas en el torrente sanguíneo. La hemofilia es un trastorno de este tipo, causado por la falta de proteínas coagulantes de la sangre. Estos pacientes han sido tratados durante mucho tiempo por la infusión de las proteínas de coagulación que faltan, pero este tratamiento es extremadamente caro y requiere inyecciones casi diarias. La terapia génica es muy prometedora para estos pacientes, ya que la sustitución del gen que hace que la proteína desaparecida podría eliminar permanentemente la necesidad de inyecciones de proteínas. Realmente no importa qué tejido produce estos factores de coagulación, siempre y cuando la proteína se entrega al torrente sanguíneo, por lo que los investigadores han tratado de entregar estos genes al músculo y al hígado utilizando varios vectores diferentes. Los enfoques que usan adenovirus recombinantes para administrar el gen del factor de coagulación al hígado son especialmente prometedores y las pruebas han demostrado una mejora clínica significativa en un modelo de hemofilia de perro.
Las enfermedades genéticas de ganancia de función presentan un desafío muy diferente porque el gen o genes mutantes crean una nueva actividad biológica que interfiere activamente con el funcionamiento normal de la célula. Un ejemplo de un trastorno de este tipo es la enfermedad de células falciformes. Los pacientes que sufren de esta enfermedad tienen una proteína de hemoglobina defectuosa en sus glóbulos rojos. Esta proteína defectuosa puede causar que sus glóbulos rojos sean deformes, obstruyendo sus vasos sanguíneos y causando coágulos de sangre extremadamente dolorosos y peligrosos. La mayoría de nuestros genes hacen una transcripción de ARN, que luego se utiliza como un modelo para hacer proteínas. En la enfermedad de células falciformes, la transcripción del gen mutante necesita ser destruida o reparada con el fin de prevenir la síntesis de hemoglobina mutante.
La reparación molecular de estas transcripciones es posible utilizando moléculas especiales de ARN llamadas ribozimas. Hay varios tipos diferentes de ribozimas: algunos que destruyen sus objetivos, y otros que modifican y reparan sus transcripciones objetivo. El método de reparación se probó en el laboratorio en células que contenían la mutación de células falciformes, y fue bastante exitoso, reparando una fracción significativa de los transcritos mutantes. Mientras que los pacientes no pueden todavía ser tratados usando esta técnica, el acercamiento ilustra cómo las moléculas que dañan biológico pueden ser inactivadas. Se están desarrollando enfoques similares para tratar las infecciones por VIH-SIDA, y éstas pueden ser utilizadas un día junto con otras terapias antivirales para tratar esta temida enfermedad.
Cáncer
Se usan estrategias muy diferentes de terapia génica para tratar el cáncer. Cuando se tratan enfermedades como la distrofia muscular, los investigadores tratan de administrar genes sin detección por el sistema inmunológico del paciente. Cuando se trata el cáncer, el objeto suele ser precisamente lo contrario: estimular la reacción inmune del paciente al tejido tumoral y mejorar su capacidad para combatir la enfermedad. Por esta razón, el tejido tumoral es a menudo transformado por el nuevo gen para producir activadores específicos del sistema inmune, tales como interleucinas o GM-CSF (factor de estimulación de colonias de monocitos de granulocitos).
Normalmente, las células cancerosas no son reconocidas por el sistema inmunológico porque son de muchas maneras idénticas a las células normales del paciente. Estos factores estimulantes activan el sistema inmunológico y ayudan a reconocer y atacar el tejido tumoral. En otro enfoque, denominado “terapia suicida”, se transfiere al tumor un gen tal como el gen de la timidina quinasa del virus del herpes simple (HSV-TK). Este gen normalmente no ocurre en el cuerpo humano, y no es metabólicamente activo. Después de varias rondas de terapia génica han acumulado altos niveles de actividad de TK en el tumor, un medicamento llamado ganciclovir se da al paciente. Este fármaco es inactivo en las células normales, pero el gen TK lo convierte en una potente toxina, matando las células tumorales. Incluso las células tumorales cercanas que no tienen el gen TK pueden ser destruidas por un fenómeno llamado “efecto espectador”. Este enfoque no sólo mata las células tumorales directamente, sino que también activa el sistema inmunológico para atacar aún más al tumor.
La terapia génica anticancerígena es un poderoso complemento de otras formas más tradicionales de tratamiento del cáncer. Sus ventajas son que puede ser beneficioso incluso si sólo una parte de las células tumorales reciben el gen transferido, no hay necesidad de expresión génica a largo plazo, y funciona con el sistema inmunológico, en lugar de intentar vencerlo. la terapia génica contra el cáncer ya está en uso significativo en la clínica, y es probable que se convierta en algo común, incluso en un futuro próximo.
A partir de estos ejemplos, debe quedar claro que se han intentado muchos enfoques diferentes de la terapia génica para la distrofia muscular, pero que cada enfoque sufre de uno o más defectos claves. Además, todos estos enfoques para tratar la distrofia muscular se enfrentan a un problema común: Aunque es fácil transferir genes a una pequeña parte de un solo músculo, simultáneamente entregar un gen a todas las partes de todos los músculos del cuerpo es imposible con la actual tecnología.
En resumen, la terapia génica abarca varias áreas relacionadas de la investigación y el tratamiento clínico, todos los que utilizan el ADN del material genético como un fármaco. La terapia génica se está utilizando actualmente, junto con otras técnicas, para tratar el cáncer. Un día, la terapia génica también puede usarse para tratar una variedad de enfermedades hereditarias y no hereditarias, que van desde trastornos de pérdida de función tales como distrofia muscular y hemofilia hasta trastornos de ganancia de función tales como enfermedad de células falciformes, enfermedades virales Como el VIH-SIDA. Áreas activas de investigación incluyen mejoras en los métodos de entrega de genes a los tejidos individuales y las células del cuerpo y la modulación de la respuesta inmune a la entrega de genes. Todavía quedan muchos desafíos para el éxito de la maduración de la terapia génica desde el laboratorio hasta el entorno clínico.
Terapia génica para el cáncer de mama
Una novedosa innovación en el tratamiento del cáncer salió a la luz en un nuevo estudio que ayuda a comprender algunos de los procesos que controlan cómo se diseminan los cánceres de seno e identifica un patrón de actividad genética que podría utilizarse para identificar a las mujeres particularmente en riesgo.
El cáncer de mama se caracteriza por una serie de mutaciones genéticas y, por lo tanto, es ideal para la intervención de terapia génica. El objetivo de la terapia génica es administrar un fármaco basado en ácido nucleico para corregir o destruir las células que albergan la aberración genética.
De acuerdo con el Instituto de Investigación del Cáncer (ICR) en Londres, que llevó a cabo la investigación, los patrones específicos de la actividad genética pueden desempeñar un papel importante para permitir que las células de cáncer de mama se diseminen por todo el cuerpo. Una vez que esto sucede, a menudo es fatal.
El estudio analizó los tumores de casi 2.000 pacientes con cáncer de mama. Se centraron en los cánceres de mama HER-2 positivos, que representan alrededor del 20 por ciento de los cánceres de mama, y encontraron que los pacientes cuyos tumores tenían actividad alta en un gen llamado F12, pero baja actividad en un gen llamado STC2, tenían tres veces más probabilidades de mueren dentro de 10 años, en comparación con pacientes con diferentes patrones de actividad en estos dos genes.
Mutaciones génicas ejemplos
Enfermedad de células falciformes y paludismo
La enfermedad de células falciformes (ECF), así llamada debido a su característico efecto antifúngico sobre los glóbulos rojos, generalmente se manifiesta a través de coágulos sanguíneos, anemia y episodios de dolor conocidos como “crisis de células falciformes”. Aunque muchos de estos síntomas pueden ser tratados con medicamentos, aún así disminuyen significativamente la calidad de vida de sus portadores.
Aunque se considera rara y una mutación, la ECF está relativamente bien investigada. Tiene lugar en el cromosoma 11, y es catalizada por la herencia de un gen anormal de la hemoglobina de ambos padres. En cuanto a la prevalencia mundial, la ECF es la más prevalente entre las poblaciones de África Occidental, con una tasa de incidencia de alrededor del 4,0%.
Las investigaciones sugieren que la prevalencia de la ECF en África Occidental no es un fenómeno fortuito. A pesar de sus efectos sobre la salud, también se ha demostrado que la ECF reduce el riesgo de contraer malaria por mosquitos. A medida que el clima de África Occidental permite que el paludismo prospere, la ECF sirve como un medio para proteger a la población.
En general, la MCS sirve como un ejemplo de mutación genética que beneficia a las poblaciones a las que afecta. Esto, en parte, es la razón por la que algunas mutaciones genéticas perduran durante décadas e incluso siglos.
Klinefelter’s Calicos
El síndrome de Klinefelter, también conocido como síndrome de Klinefelter XXY, es una mutación genética en la cual un sujeto masculino lleva un cromosoma X adicional, por lo tanto lleva el genotipo femenino XX además del genotipo masculino XY tradicional. Del mismo modo, los hombres con el síndrome de Klinefelter a menudo tienen rasgos femeninos, como tejido mamario, y es posible que no puedan reproducirse.
Como se encuentra en el código genético, que es homólogo entre la mayoría de las especies, el síndrome de Klinefelter no es exclusivo de los humanos. Por lo tanto, gatos, perros e incluso ballenas pueden heredar el genotipo XXY.
En los gatos, el cromosoma X contiene más información que la relacionada con el sexo. El color de la piel, por ejemplo, se transmite por el cromosoma X.
Además, el color de la piel es codominante. Dado que los gatos de sexo masculino suelen heredar sólo un cromosoma X y las gatas de sexo femenino dos cromosomas X, es más probable que las gatas tengan patrones de pelo multicolores que los gatos de sexo masculino.
Esto es especialmente cierto para el calico, un gato conocido por su llamativo pelaje naranja y negro. El gen para el pelo negro no puede ser transmitido en el mismo cromosoma X que el gen para el pelo anaranjado, que hace que los gatos calicos sean casi exclusivamente hembras.
Sin embargo, esto no hace imposible la existencia de un calicó masculino. Los gatos machos con dos cromosomas X, o genotipo XXY, pueden ser portadores del gen del pelaje anaranjado en un cromosoma X y del gen del pelaje negro en el otro. De esta manera, son realmente “Calicos de Klienfelter”.
Tolerancia a la lactosa
Mencionamos anteriormente cómo la ECF, una mutación marcada por síntomas físicos que a veces ponen en peligro la vida, también funciona para prevenir la malaria en África Occidental. La tolerancia a la lactosa es otra mutación que beneficia a quienes la tienen.
Originalmente, el cuerpo humano era incapaz de producir lactasa, una enzima que digiere las proteínas de la leche de vaca, después de los primeros meses de vida. Esto se debe a que los seres humanos a menudo no consumían leche – u otros productos lácteos, para el caso – en la edad adulta.
El aumento de la pasteurización, así como la agricultura comercial, casi acabó con este viejo hábito. Como podemos ver hoy en día, los seres humanos de todas las edades comen queso y beben leche. Por supuesto, esto viene después de un cambio corporal significativo. Una mutación que prolonga la producción de lactasa en humanos, que actualmente es más prevalente en los países occidentales, permite a los humanos comer productos lácteos sin dolor de estómago ni náuseas.
Al igual que la ECF, esta mutación permanece porque ayuda a los humanos a consumir nutrientes vitales, como el calcio y el potasio, a través de una gama más diversa de fuentes.
Tema que te puede interesar : Tatuajes temporales cuanto duran